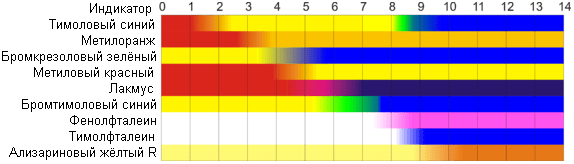
Естествени pH индикатори
Под влияние на промените в реакцията на околната среда не само съединенията, използвани в лабораториите като индикатори, придобиват различни цветове. Също толкова многобройна група е съставена от вещества, съдържащи се в естествените продукти. В няколко опита ще тестваме поведението на pH индикаторите в нашата среда.
За експерименти ще са необходими няколко разтвора с различно pH. Те могат да бъдат получени чрез разреждане на солна киселина с HCl (pH 3-4% разтвор е 0) и разтвор на натриев хидроксид NaOH (4% разтвор има pH 14). Дестилираната вода, която също ще използваме, е с pH 7 (неутрално). В изследването ще използваме сок от цвекло, сок от червено зеле, сок от боровинки и запарка от чай.
В епруветки с приготвени разтвори и дестилирана вода капнете малко сок от червено цвекло (снимка 1). В киселинни разтвори придобива интензивен червен цвят, в неутрални и алкални разтвори цветът става кафяв, превръщайки се в жълт оттенък (снимка 2). Последният цвят е резултат от разлагането на багрилото в силно алкална среда. Веществото, отговорно за обезцветяването на сока от цвекло, е бетанин. Подкисляването на борш или салата от цвекло е кулинарен „чип“, който придава на ястието апетитен цвят.
По същия начин опитайте сок от червено зеле (снимка 3). В кисел разтвор сокът става яркочервен, в неутрален - светло лилав, а в алкален - зелен. И в този случай силната основа разлага багрилото - течността в епруветката става жълта (снимка 4). Веществата, които променят цвета си, са антоцианини. Поръсването на салата от червено зеле с лимонов сок придава привлекателен вид.
Друг експеримент изисква сок от боровинки (снимка 5). Червено-виолетовият цвят се променя в червено в кисела среда, в зелено в алкална среда и в жълто в силно алкална среда (разлагане на багрилото) (снимка 6). И тук антоцианините са отговорни за промяната на цвета на сока.
Чаената инфузия може да се използва и като индикатор за pH на разтвора (снимка 7). В присъствието на киселини цветът става сламеножълт, в неутрална среда става светлокафяв, а в алкална среда става тъмнокафяв (снимка 8). Производните на танина са отговорни за промяната на цвета на запарката, придавайки на чая характерния тръпчив вкус. Добавянето на лимонов сок прави цвета на запарката по-светъл.
Струва си също да се провеждат самостоятелно тестове с други естествени показатели - много сокове и отвари от растения променят цвета си поради подкиселяване или алкализиране на околната среда.
Вижте го във видеото:
Естествени pH индикатори
